- PDNレクチャーとは?
- Chapter1 PEG
- Chapter2 経腸栄養
- 1.経腸栄養の特徴と適応
- 2.経腸栄養剤の分類
- 3.病態別経腸栄養剤
- 3.1 病態別経腸栄養剤とは?
- 3.2 肝不全用栄養剤
- 3.3 腎不全用栄養剤
- 3.4 糖尿病用栄養剤
- 3.5 呼吸不全用栄養剤
- 3.6 免疫賦活栄養剤、免疫調節栄養剤
- 4.経腸栄養に用いられる製剤および食品
- 4.1 グルタミン製剤(食品)
- 4.2 微量元素製剤
- 4.3 食物繊維
- 4.4 プロバイオティクス、シンバイオティクス
- ① プロバイオティクス
- ② シンバイオティクス
- 4.5 ORS(経口補水液)
- 4.6 増粘剤、ゲル化剤
- 4.7 脂肪酸
- ① 脂肪酸とその分類
- ② 多価不飽和脂肪酸(ω-3, ω-6系)
- ③ 中鎖脂肪酸(MCT)
- 5.半固形化栄養剤
- 5.1 基礎的な知識
- 5.2 臨床的な知識
- ①胃瘻からの半固形化栄養材
短時間注入法 - ②栄養剤形状機能について
- 6.ミキサー食
- 6.1 ミキサー食(成人)
- 6.2 ミキサー食(小児)
- 6.3 ミキサー食(小児)
- 7.早期経腸栄養
- 8.周術期経腸栄養
- 9.在宅経腸栄養
- 9.1 在宅経腸栄養
- 9.2 在宅診療の医療費の実際
- 9.3 終末期医療にかかる費用
- 10.経腸栄養に必要な器具
- 11.経腸栄養時の薬剤投与
- 12.経腸栄養の管理
- 13.経腸栄養の合併症と対策
- 14.栄養剤使用時の栄養アセスメント
- ●「経腸栄養」関連製品一覧
- Chapter3 静脈栄養
- Chapter4 摂食・嚥下リハビリ
- PDNレクチャーご利用にあたって



Chapter2 経腸栄養
3.病態別経腸栄養剤
5.呼吸不全用栄養剤
苫小牧市立病院 副院長 河内正治

2015年10月22日改訂
<Point>
- 呼吸不全患者においては、他の疾患と異なり、呼吸不全病態においてはその重症度が必要代謝量(エネルギー量)の決定に大きく関与しているため、重症であればあるほどきちんとした栄養評価が必要である。
- 吸不全患者においては必要エネルギー量が相対的に多くなるが、疾患としては水分量を制限する必要があり、高度の呼吸不全時にはカロリー投与量と全体の水分量のバランスに充分注意して経腸栄養剤を選択する必要がある。
- 換気障害(PaCO2の上昇を伴う二酸化炭素蓄積)を伴う重症呼吸不全患者においては、呼吸負荷を軽減するために、可能な限り二酸化炭素の発生を抑えるような経腸栄養剤を選択することが望ましい。
- 免疫強化栄養剤については、強化されているものについて評価が定まっていないことも多く、病態に合わせて使用する。
- 必ずしも投与量全量を同一の栄養剤で賄う必要はなく、呼吸不全は病態の幅が広いので、病態や患者個人に合わせて適宜調整する。
1.投与量を決める
1.1 呼吸不全患者における特徴
投与カロリー量(必要カロリー量)を決定するには栄養評価を行なう。呼吸不全患者では病態に応じて消費カロリー量が変動するので、病態/栄養状態の評価は非常に重要である。慢性呼吸器疾患(COPDなど)では、安定した状態と入院が必要な急性増悪時とでは全く必要カロリー量が異なる。また、急性増悪状態においても自発呼吸の状態と人工呼吸管理下では大きく必要代謝量が異なる。適切なカロリー投与は治療上大きな意味を持ち、量が足りないともちろん栄養不良を生じるが、投与量が必要量を超えて肝腎負荷や水分負荷をかけることもしばしば重大な結果をもたらすので、適切な必要量の評価には大いに注意が必要である。
1.2 呼吸に必要なエネルギー
呼吸は、循環系(心臓)と並んで最も基本的な運動(生命維持に必須)であり、呼吸に使用される筋肉(横隔膜と内・外肋間筋)は、毎分10回以上の収縮/伸展を繰りかえす。そのため正常な呼吸にも大きなエネルギーを必要とし、この呼吸に必要なエネルギーは基礎代謝量として算出される。健康成人においてはおよそ基礎代謝量の1/4~1/5が呼吸仕事量とされるので、自発呼吸に使われるエネルギー量はおよそ200~250kcal/日で計算することが一般的である1)。
1.3 急性増悪時はなぜ必要カロリー量が増加する?
呼吸困難や呼吸不全が生じると上記の呼吸筋のほかに、補助呼吸筋群として腹直筋およびほぼすべての顔面頚部胸部にある筋肉が動員される。動員する筋肉量のみならず胸腔内を陰圧にする力や呼吸回数が増加するために、呼吸筋の消費エネルギー量は増大し、さらに酸素の運搬量を維持するために循環系の仕事量も飛躍的に増加する。この結果、大雑把には、分時換気量が二倍になれば(例えば呼吸回数が25回の患者)呼吸に要する仕事量は全体として4倍近くになる2)。
1.4 安定期と急性増悪時(自発呼吸時)の必要エネルギー量の差は?
同一疾患の慢性呼吸不全症例(肺非結核性抗酸菌症)で、病状が安定していて外来通院中の患者と、入院が必要になった(病態が増悪したが人工呼吸管理は必要としていない)患者間において、安静時代謝量の実測値(間接的熱量測定法を用いて計測)と計算値(ハリスベネディクトの式(Harris-Benedict equation;以下HB式)より計算した基礎代謝量3)×1.1)に乖離があるかを比較検討した(図1)。
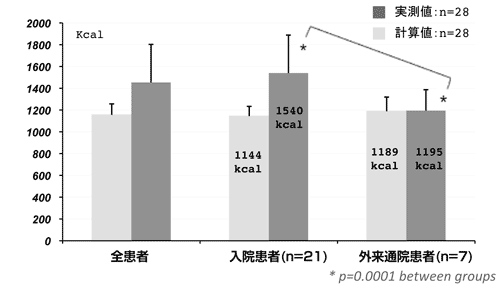
外来通院患者群では実測値と計算値の間に有意差を認めなかったが、入院患者群においては約400kcalほど有意差が生じ、かつ外来患者群に対しても群間で有意差を示した。患者背景因子を調べると(表1)、呼吸回数が入院患者で有意に多く(入院患者68、外来患者48回/3分間)、呼吸仕事量の増加がこのREE増の原因であると考えられた。このように慢性呼吸器疾患では安定時と悪化した場合は必要エネルギー量が大きく異なる。具体的には、急性増悪時にはストレス係数を約1.4(安定期には1.1)として計算すると正しい値が得られることになる。
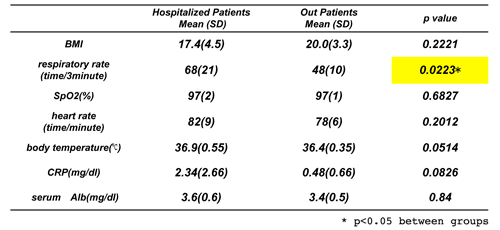
1.5 人工呼吸管理中の必要エネルギー量
上述の呼吸仕事量が増大した必要エネルギー量の増加部分は、いったん人工呼吸管理になると激減する。もし調節呼吸であれば呼吸仕事量が理論上はゼロなので、基礎代謝量は「HB式で得られた計算値」×0.8になり、自発呼吸下急性増悪時の半分以下になるので、投与量の変化に注意する4)。
2.何を投与するか?
2.1 エネルギー基質
2.1.1 エネルギー源となる基質
人のエネルギー源となる摂取物を熱量素(三大栄養素)といい、糖質/脂質/タンパク質のことである。それぞれ1グラム当たりに発生する熱量は異なり、人においての有効熱量は一般に、糖質(炭水化物)/脂質/タンパク質それぞれ4/9/4 kcalである。したがって単位重量当たりでもっともエネルギー源として効率が良いのは脂質である。
2.1.2 呼吸商と二酸化炭素排出量
糖質/脂質/タンパク質、いずれも体内で燃焼して酸素を消費して二酸化炭素と水とエネルギー(カロリー)を生じる。単位量当たりに産生される二酸化炭素量を消費される酸素で除した値を呼吸商(RQ: respiratory quotient)といい、この値が1であれば、取り込んだ酸素と同量の二酸化炭素が排出されることになる。ところが、このRQは基質によって異なり、糖質/脂質/タンパク質ではそれぞれ1/0.7/0.84(概算値)である。したがって、同量のカロリーを得る場合に脂質は炭水化物の1/3以下の二酸化炭素しか排出しない。
2.1.3 高脂肪/低炭水化物(High fat & low CHO)経腸栄養
そこで、高脂肪/低炭水化物(High fat & low CHO)経腸栄養が作られたが、重症呼吸不全患者に対して高脂肪/低炭水化物とした経腸栄養を推奨する十分なデータは得られていない。しかし、COPD の急性増悪による呼吸不全患者における人工呼吸期間の短縮や酸素化能の改善に役立つ可能性はある5)。
2.1.4 呼吸不全患者と投与量
呼吸不全患者では、一般に同年齢健常人より必要カロリー量が多くなるが、逆に水分過多は肺疾患に良くない。そこで、1グラム当たりのカロリー量が多い栄養剤を使用するなど、投与量を増やしても摂取水分量を増加させない工夫が必要である。
2.2 脂質
2.2.1 n-3 系脂肪酸とn-6 系脂肪酸
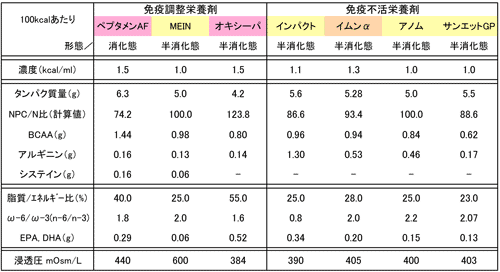
不飽和脂肪酸にはω-3/ω-6/ω-9(n-3/n-6/n-9)系がありそれぞれ最終代謝産物が異なる。n-6 系脂肪酸からはPGE2、TXA2、LTB4 などの炎症性メディエーターが産生され、これらが過剰に産生されると全身炎症性症候群(SIRS: systemic inflammatory response syndrome)等の重篤な炎症反応を引き起こす可能性がある。他方n-3 系脂肪酸からはPGE3、TXA3、LTB5 などが産生され、それらと競合的に働く。また、n-3 系脂肪酸は炎症の収束を促す代謝物(Resolvins、Protectins)へ変化するともいわれている。これらn-3 系脂肪酸が持つ抗炎症作用が呼吸不全患者に良いことが知られている6)。実際にn-3系を強化した栄養剤が最近では多く発売されている(表2 免疫栄養剤)。

2.2.2 EPA(エイコサペンタ酸)とDHA(ドコサヘキサエン酸)
n-3 系脂肪酸の代表はEPAとDHAであり、ともに魚油食品や青魚に多く含まれる。同じくn-3系であるALA(α-リノレン酸)と合わせて必須脂肪酸であるが、AHAから体内で合成することも可能である。特にEPAを強化した栄養剤が呼吸不全(ARDS/ALI)の治療に効果あることや、敗血症症例で酸素可能を改善することなどが示されている7)。
2.3 タンパク質
2.3.1 アルギニン
アルギニン強化免疫調整栄養剤は軽度・中等度の敗血症では安全であるが、高度の敗血症患者に使用された場合は危険となりうるとされている。同様に、呼吸不全患者において感染症合併率を低下させるという報告もあるが、はっきりしていない。
2.3.2 グルタミン
グルタミンは抗酸化反応、免疫機能などに関与し、様々な有効性を発揮する条件付き必須アミノ酸である。消化管においては腸上皮細胞の栄養となり、腸管のintegrity を維持する。したがってグルタミン強化栄養剤は呼吸不全例においても有効である可能性はある。これまでの報告から推奨投与量は0.3~0.5g/kg/day とされている。
2.3.3 投与量(NPC/N比)
呼吸不全患者での至適タンパク質投与量は、窒素投与量として0.24gN/kg/day、タンパク質に換算して1.5g/kg/day であると考えられている。標準的な経腸栄養剤では非タンパク質カロリー窒素比(NPC/N)が150 以上と高く、重症病態の症例に使用時には、表記の投与量を目指しタンパク質追加による補正を行う必要がある。食品ではタンパク質を強化した栄養剤が発売されている(↑表2 免疫栄養剤)。
3.投与する製品としては何を選択する?
これまで議論してきたことから明らかなように、投与エネルギー量を増加し、しかも呼吸仕事量を減らすべく二酸化炭素負荷を減らし、かつ投与水分量を抑えるためには、脂質を多く用いた栄養剤が有利である。また、蛋白投与量もNPC/Nで120~130ぐらいが望ましい。さらにn-3系/アルギニンなどが強化されていた方がよいだろう。
3.1 医薬品経腸栄養剤
医薬品では、半消化態栄養剤と消化態栄養剤(成分栄養剤)がある。表3に呼吸不全症例に投与する際考慮する項目についてまとめたが、成分栄養剤は脂質において大いに不利である。濃度を考えるとエンシュア®・H以外の選択肢は無いが、他の項目を考慮するとラコール®が有利である。いずれにしても選択肢が少ないので経済的な理由等以外ではあまり積極的に医薬品を呼吸不全例に使用する意義は少ない。
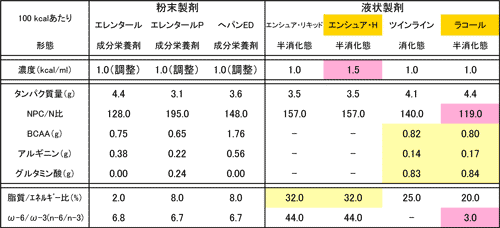
3.2 食品
食品の経腸栄養剤は非常に種類が豊富で、天然濃厚流動食/人工濃厚流動食があり選択肢が非常に多いのが特徴である。病態に特化した 治療効果を期待できる人工濃厚流動食の中では、免疫強化栄養剤がやはり有力な候補となる(表2)。
いずれもEPA/DHAが配合されてn-6/n-3比は低く、アルギニンも強化されていて重症患者に使用するのにふさわしい。なかでも呼吸不全用に開発されたオキシーパ®とペプタメン®AFは、呼吸商の点からも有利で選択肢としては最右翼である。オキシーパ®は脂質エネルギー比が55%ともっとも高く、非常に呼吸商の点からは有利でかつ水分量も押さえられているが、この点が逆に日本人では下痢を起こし易く忍容性が不良である点に注意する。ペプタメン®AFもまた脂質エネルギー比は40%と高いが、下痢を生じる率は形態が消化態ということもあってそれほど高くない。日本人は炭水化物への依存率が高いので、単剤で投与することにあまりこだわる必要はなく、いくつかの栄養剤を併用しつつ必要エネルギー量を満たすように徐々に投与量/質を調整することが大切である。
文献
- Lumb AB, et al. Pulmonary ventilation, In Nunn's Applied Respiratory Physiology. Elsevier International, pp76-89, 2005.
- Lumb AB, et al. Exercise, In Nunn’s Applied Respiratory Physiology. Elsevier International, p 242, 2005.
- Harris JA, et al. A biometric study of basal metabolism in man. Carnegie Institution of Washington, Washington D.C. Lippincott Co., Philadelphia, 1919.
- 河内 正治, ほか:人工呼吸管理中の栄養管理.日本呼吸ケア・リハビリテーション学会誌20 : 120-124, 2010.
- Mesejo A, et al : Comparison of a high-protein disease-specific enteral formula with a high-protein enteral formula in hyperglycemic critically ill patients. Clin Nutr. 22:295-305, 2003.
- Gadek JE, et al : Effect of enteral feeding with eicosapentaenoic acid, gamma-linolenic acid, and antioxidants in patients with acute respiratory distress syndrome. Crit Care Med 27:1409-1420, 1999.
- Singer P, et al : Benefit of an enteral diet enriched with eicosapentaenoic acid and gamma-linolenic acid in ventilated patients with acute lung injury. Crit Care Med 34:1033-1038, 2006.



